par Chantale | Juin 2, 2023 | Santé
Vous résidez à Paris et vous êtes face à une urgence dentaire ? Naturellement, nous compatissons. Cependant, ce dont vous avez le plus besoin est de savoir ce qu’il faut faire dans cette situation. Pour cela, nous vous proposons des solutions concises et pratiques...

par Chantale | Juin 1, 2023 | CBD
Green Owl est le meilleur fournisseur du cannabidiol issu de la plante de chanvre. La marque détient une grande boutique de vente de CBD à Toulouse qui est d’ailleurs son siège social. De plus, le détenteur du marché de CBD en France dispose également d’une boutique...
par Chantale | Mai 31, 2023 | Santé
Lorsque vous sentez de maux de dents (que ce soit en urgence ou non) il est indispensable de vous faire prendre en charge par un dentiste. Cependant, certains chirurgiens-dentistes effectuent des dépassements d’honoraires ; ce qui n’est généralement pas le cas auprès...
par Chantale | Mai 30, 2023 | Santé
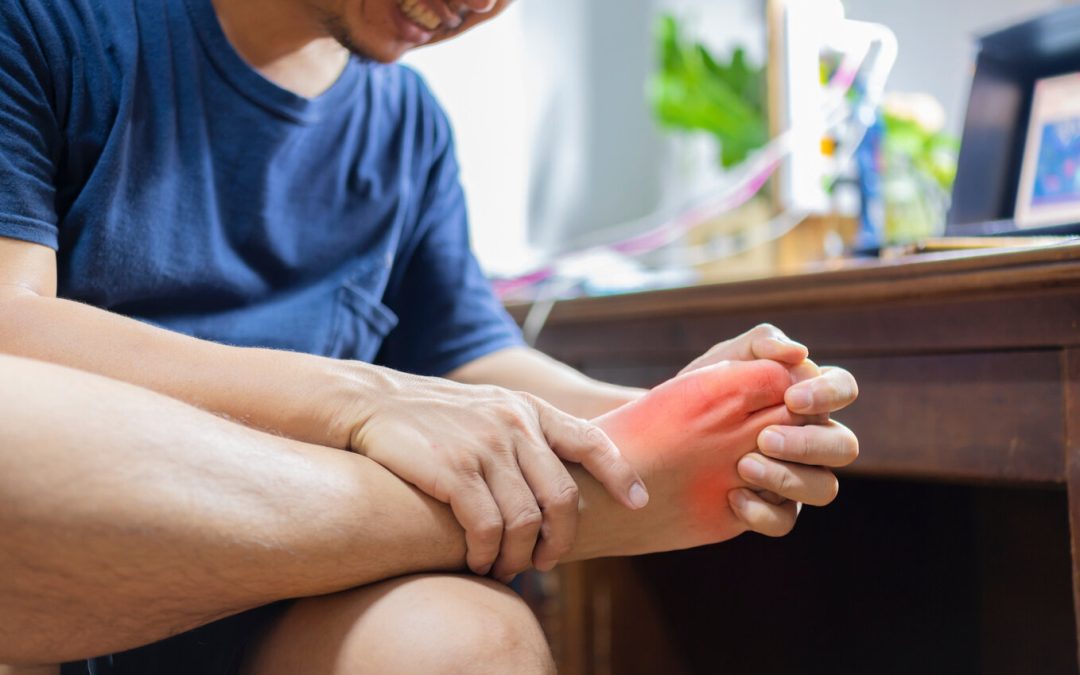
La goutte est une maladie caractérisée par le dépôt de cristaux d’acide urique dans les articulations entraînant ainsi une inflammation. L’acide urique provient de la dégradation des aliments d’origine animale. Normalement, cette substance est évacuée de...

par Chantale | Mai 24, 2023 | CBD
Le cannabidiol issu de la plante de chanvre (cannabis sativa) est reconnu pour ses vertus médicinales, notamment thérapeutiques. Il en existe sous diverses formes : gélules, huile de CBD, liquide à vapoter, bougie, crème, etc. Sous toutes ses formes, vous avez deux...

par Chantale | Mai 16, 2023 | Beauté
Le peeling du visage est un soin préventif de la médecine esthétique qui a pour mission l’élimination des couches supérieures de la peau. Cette technique permet à la peau de se renouveler. Cependant, il faut respecter un minimum de conditions pour avoir de bons...

par Chantale | Mai 16, 2023 | Santé
Un abcès dentaire peut être causé par une mauvaise hygiène bucco-dentaire. C’est une infection qui embrasse non seulement les enfants, mais aussi les adultes. Naturellement, l’abcès dentaire et joue gonflée sont liés et s’accompagnent de fortes douleurs. Cependant, la...

par Chantale | Mai 2, 2023 | Beauté
Pour apparaitre toujours rayonnant et profiter d’une bonne forme, certaines parties de votre corps telles que la peau, les ongles et les cheveux doivent être entretenues. Pour y parvenir, l’usage de certains produits est recommandé. Dans ce cas, le plus souvent, on...
par Chantale | Avr 4, 2023 | Santé
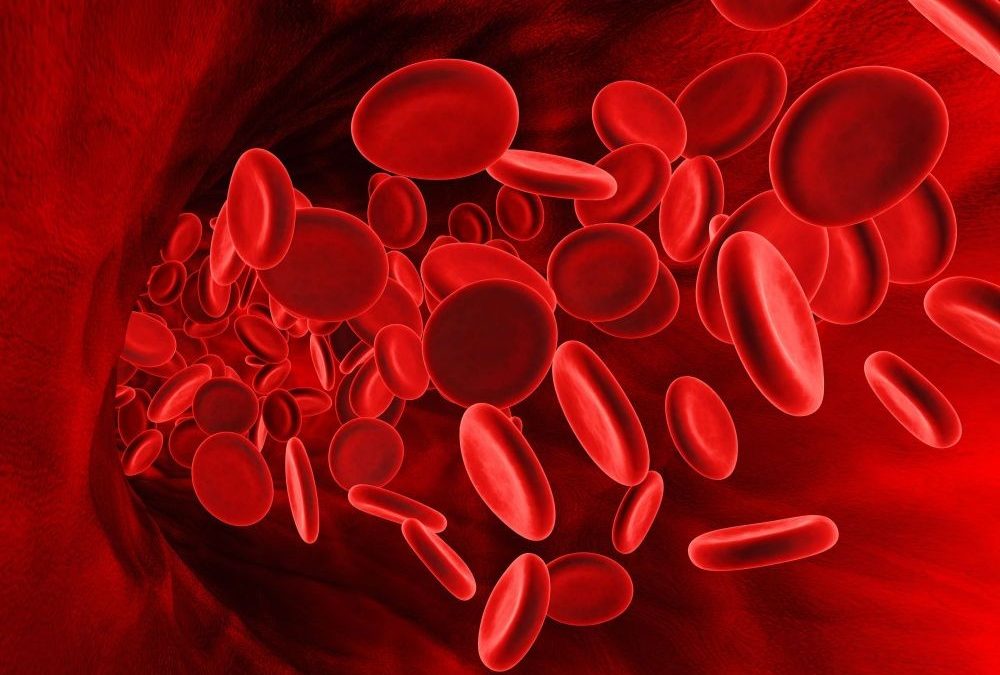
Le VGM dans une prise de sang est une mesure clé incluse dans la numération formule sanguine (NFS) effectuée lors d’une prise de sang. Cette mesure aide à déterminer le volume moyen des globules rouges dans le sang. Lisez cet article pour en apprendre davantage sur ce...

par Chantale | Avr 3, 2023 | Santé
Face à la multitude qui existe, choisir un remède de grand-mère contre l’arthrose cervicale n’est pas toujours évident. En effet, cette maladie peut être douloureuse et gênante pour les personnes âgées. Il n’existe pas de remède miracle pour cette maladie, mais...











